spécification
Taq ADN polymérase 1000 U avec tampon mixte (Expédition avec sac de glace)
Stockage Conditions:
Taq ADN polymérase et Taq RAP Les kits doivent être stockés à -30 à -15°C au congélateur à température constante dès réception.
Test:
Remarques avant de commencer:
- Fourni avec un tampon Load PCR contenant un réactif de chargement de gel et des colorants de suivi de gel.
- Le tampon PCR et le tampon PCR de charge donnent une concentration finale de 1.5 mM MgCl2 dans le mélange réactionnel. Ajuster la concentration de Mg2+ si nécessaire en ajoutant 25 mM MgCl2.
- Mélange dNTP de qualité PCR de haute qualité (10 mM) est disponible séparément si nécessaire.
- Conserver les tubes PCR sur la glace jusqu'à ce qu'ils soient placés dans le thermocycleur.
- Inclure un contrôle sans modèle (CTN) dans chaque essai.
Préparation et mixage:
- Décongeler les tampons et les réactifs à température ambiante ou sur de la glace, puis conservez-les sur la glace après décongélation complète.
- Préparer un mélange réactionnel contenant tous les composants de la PCR, à l'exception de l'ADN matrice. Préparer 10% plus de volume que nécessaire.
- Mélangez soigneusement le mélange réactionnel et versez-le dans des tubes PCR.
- Ajouter un modèle d'ADN (≤1 µg/réaction) aux tubes PCR. Pour la RT-PCR, ajouter une aliquote de la réaction de transcriptase inverse, ne dépassant pas 10% du volume final de PCR.
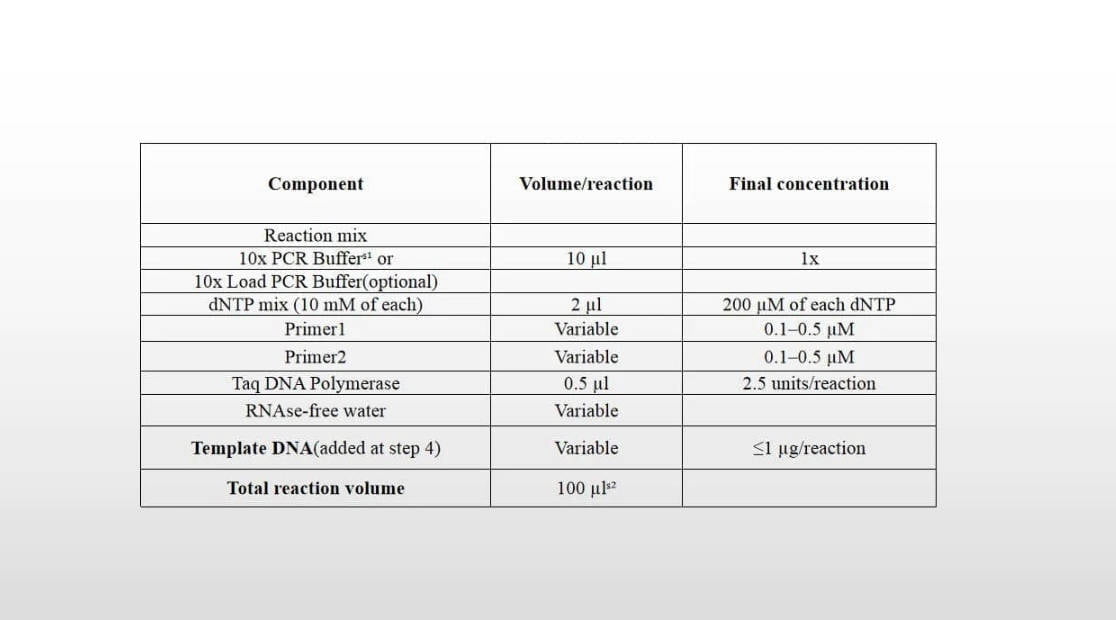
Configuration de la réaction utilisant l'ADN polymérase SENO Taq
| Composant | Volume/réaction | Concentration finale |
| Mélange réactionnel | ||
| 10x Tampon PCRˢ¹ ou | 10 µl | 1X |
| 10x Charger le tampon PCR(facultatif) | ||
| mélange dNTP (10 mM de chaque) | 2 µl | 200 µM de chaque dNTP |
| Apprêt1 | Variable | 0.1–0,5 µM |
| Apprêt2 | Variable | 0.1–0,5 µM |
| Taq ADN polymérase | 0.5 µl | 2.5 unités/réaction |
| Eau sans RNAse | Variable | |
| ADN de modèle (ajouté à l'étape 4) | Variable | ≤1 µg/réaction |
| Volume total de réaction | 100 µlˢ² |
Thermique Vélo:
Programmer le thermocycleur selon les instructions du fabricant. Référez-vous au programme de cyclisme fourni.
Conditions de cyclage optimisées pour la Taq ADN polymérase
| Étape | Temps | Température | Commentaire |
|---|---|---|---|
| Dénaturation initiale | 3 min | 94°C | |
| 3-étape à vélo: | |||
| Dénaturation | 0.5–1 min | 94°C | |
| Recuit | 0.5–1 min | 50–68°C | Environ 5°C en dessous de la Tm des amorces. |
| Extension | 1 min | 72°C | Pour les produits PCR plus longs que 1 ko, utiliser une durée de prolongation d'environ 1 min par Ko d'ADN. |
| Nombre de cycles | 25–35 | ||
| Prolongation définitive | 10 min | 72°C |
Simplifié Démarrage à chaud:
Démarrer le programme PCR. Une fois que le thermocycleur atteint 94°C, placer les tubes PCR dans le cycleur pour une spécificité améliorée.
Post-PCR:
- Après amplification, les échantillons peuvent être conservés entre 2 et 8 °C pendant la nuit ou à -20 °C pour une conservation plus longue.
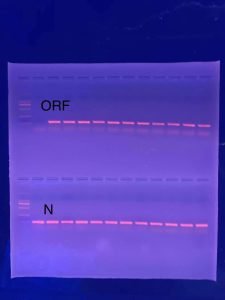
- Les produits PCR peuvent être directement chargés sur du gel d'agarose à l'aide du Load PCR Buffer sans ajout préalable de tampon de chargement et de colorants de suivi du gel.. Reportez-vous au tableau fourni pour connaître la distance de migration et les colorants de suivi du gel..
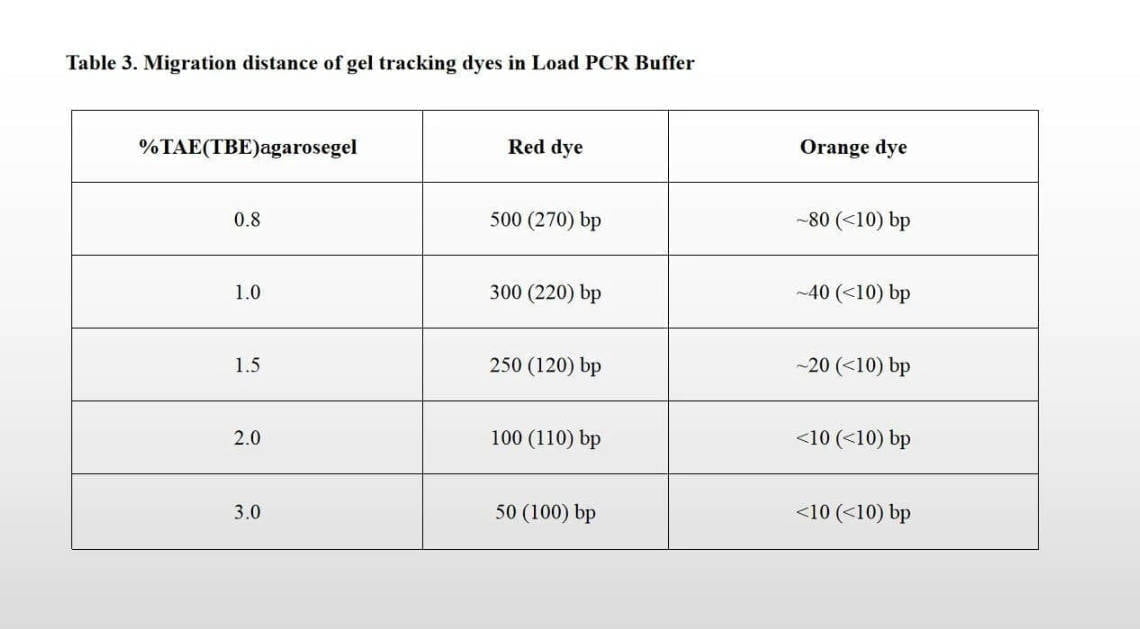
Distance de migration des colorants de suivi du gel dans le tampon Load PCR
| % TAE (TBE) ungarose gel | Colorant rouge | Colorant orange |
| 0.8 | 500 (270) pb | ~80 (<10) pb |
| 1.0 | 300 (220) pb | ~40 (<10) pb |
| 1.5 | 250 (120) pb | ~20 (<10) pb |
| 2.0 | 100 (110) pb | <10 (<10) pb |
| 3.0 | 50 (100) pb | <10 (<10) pb |









Commentaires
Il n'y a pas encore de critiques.