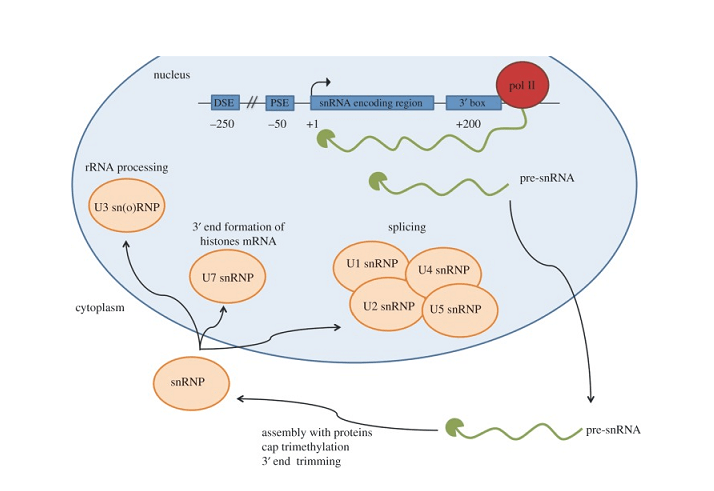
RNAs นิวเคลียร์เดี่ยว, หรือ snrnas, มีบทบาทสำคัญภายในเซลล์แม้จะมีความยาวสั้น ๆ. เนื่องจากโมเลกุล RNA ที่ไม่มีการเข้ารหัสพบได้ในนิวเคลียสเท่านั้น, snRNAs มีส่วนร่วมในการดัดแปลงหลังการถอดรหัสที่จำเป็นซึ่งช่วยสังเคราะห์โปรตีนที่ใช้งานได้. snRNA มีสองคลาสหลัก – ยู1, ยู2, ยู4, ยู5, และ U6 ซึ่งก่อตัวเป็นไรโบนิวคลีโอโปรตีนนิวเคลียร์ขนาดเล็ก (snRNP) มีส่วนร่วมในการประกบ, และกล่อง snoRNA ของ H/ACA และ C/D ซึ่งเป็นแนวทางในการดัดแปลงทางเคมีของ RNA อื่นๆ.
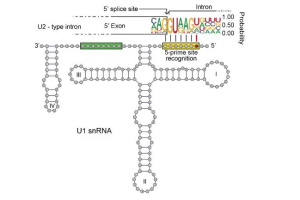
การจัดลำดับ RNA นิวเคลียสเดี่ยวคืออะไร (snRNA-seq)?
การจัดลำดับ RNA นิวเคลียสเดี่ยว, หรือ snRNA-seq, เป็นเทคนิคเชิงนวัตกรรมในการวิเคราะห์นิวเคลียสทรานสคริปโตมที่แยกได้จากเซลล์แต่ละเซลล์. แนวทางนี้ช่วยลดการตอบสนองความเครียดจากการถอดเสียงที่อาจบิดเบือนผลลัพธ์ระหว่างการแยกตัวออกจากกัน. เมื่อเปรียบเทียบกับการจัดลำดับ RNA เซลล์เดียวแบบดั้งเดิม (scRNA-seq), snRNA-seq จัดแสดงประโยชน์บางประการที่ช่วยเพิ่มอรรถประโยชน์ในการตรวจสอบความหลากหลายของเซลล์.
ความแตกต่างระหว่าง snRNA-seq และ scRNA-seq คืออะไร?
การจัดลำดับ RNA นิวเคลียสเดี่ยว (snRNA-seq), หรือที่เรียกว่า snRNA-seq หรือ sNuc-seq, เป็นวิธีการจัดลำดับ RNA ที่เป็นนวัตกรรมใหม่ที่ใช้ในการจัดโปรไฟล์การแสดงออกของยีนในเซลล์ที่ยากต่อการแยก. เทคนิคนี้เป็นทางเลือกที่มีประสิทธิภาพในการจัดลำดับ RNA เซลล์เดียว (scRNA-seq) โดยการวิเคราะห์นิวเคลียสแทนเซลล์ที่สมบูรณ์. แต่สิ่งที่ทำให้ snRNA-seq แตกต่างจาก scRNA-seq อย่างแน่นอน? มาเจาะลึกถึงความแตกต่างที่สำคัญกัน.
scRNA-seq วัดทั้งการถอดเสียงไซโตพลาสซึมและนิวเคลียร์, ให้มุมมองที่ครอบคลุมเกี่ยวกับโปรไฟล์การแสดงออกของยีนของเซลล์. ในทางตรงกันข้าม, snRNA-seq จะวัดการถอดเสียงนิวเคลียร์เป็นหลัก, เนื่องจากมุ่งเน้นไปที่การวิเคราะห์ RNA ภายในนิวเคลียสนั่นเอง. วิธีการกำหนดเป้าหมายนี้ช่วยลดการเกิดการแสดงออกของยีนปลอมให้เหลือน้อยที่สุด, เนื่องจากไรโบโซมที่โตเต็มที่จะอาศัยอยู่ในไซโตพลาสซึม. ดังนั้น, ปัจจัยการถอดรหัสใด ๆ ที่แสดงออกมาหลังจากกระบวนการแยกตัวไม่สามารถแปลได้, ป้องกันการถอดรหัสเป้าหมายดาวน์สตรีม.
snRNA-seq รองรับประเภทเนื้อเยื่อที่ท้าทายได้อย่างไร?
สำหรับหนึ่ง, snRNA-seq รองรับเนื้อเยื่อได้หลากหลายประเภทซึ่งอาจเป็นเรื่องยากที่จะแยกตัวออกเป็นเซลล์เดียวอย่างสมบูรณ์. เนื้อเยื่อที่ซับซ้อนซึ่งมีเมทริกซ์นอกเซลล์หนาแน่นเช่นสมอง, ไต, และหัวใจสามารถวิเคราะห์ได้อย่างมีประสิทธิภาพมากขึ้นโดยใช้ snRNA-seq เนื่องจากโปรโตคอลการแยกตัวที่เบากว่า. สิ่งนี้จะรักษาความสมบูรณ์ของเซลล์ประเภทละเอียดอ่อนที่อาจได้รับการเปลี่ยนแปลงหรือลดระดับลงในระหว่างการแยกตัวที่รุนแรงขึ้นซึ่งจำเป็นสำหรับ scRNA-seq.
ประโยชน์ของการใช้ snRNA-seq สำหรับตัวอย่างที่เก็บถาวรคืออะไร?
SnRNA-seq ยังสนับสนุนการศึกษาตัวอย่างทางคลินิกที่เก็บถาวร. เนื้อเยื่อที่แช่แข็งหรือคงที่ซึ่งเข้ากันไม่ได้กับ scRNA-seq สามารถจัดทำโปรไฟล์ได้ตราบเท่าที่สามารถแยกนิวเคลียสที่ไม่บุบสลายได้. สิ่งนี้จะขยายขอบเขตของการประยุกต์ใช้การวิจัยที่เป็นไปได้ เมื่อเทียบกับวิธีการจัดลำดับอื่นๆ ที่ต้องการเซลล์เดี่ยวที่แยกออกมาใหม่. สะดุดตา, snRNA-seq ช่วยให้นักวิจัยสามารถวิเคราะห์เนื้อเยื่อสมองของมนุษย์หลังการชันสูตรพลิกศพ เพื่อค้นหาความหลากหลายของเส้นประสาทในระดับเซลล์เดียว.
snRNA-seq มีมุมมองที่เป็นเอกลักษณ์อะไรบ้าง?
แทนที่จะเป็นมุมมองที่ครอบคลุมของการถอดเสียงแบบเต็ม, snRNA-seq ให้ข้อมูลเชิงลึกที่มุ่งเน้นเกี่ยวกับกระบวนการนิวเคลียร์และการโต้ตอบที่ปรับโดย snRNA. โดยนำเสนอมุมมองที่ขยายออกไปอย่างมีเอกลักษณ์เกี่ยวกับกลไกการกำกับดูแลภายในพื้นที่นิวเคลียร์อันจำกัด. การใช้ snRNA-seq กับตัวอย่างเนื้อเยื่อที่ซับซ้อนได้เปิดเผยประเภทเซลล์ใหม่และสถานะที่อาจตรวจไม่พบโดยใช้ scRNA-seq เพียงอย่างเดียว. การค้นพบดังกล่าวทำให้เรามีความเข้าใจลึกซึ้งยิ่งขึ้นเกี่ยวกับการจัดระเบียบและความเชี่ยวชาญด้านเซลลูล่าร์, ขยายขอบเขตของการแพทย์เฉพาะทาง.
snRNA-seq สามารถช่วยโปรไฟล์การแสดงออกของยีนในกลุ่มตัวอย่างที่ท้าทายได้อย่างไร?
ความสามารถในการจัดทำโปรไฟล์นิวเคลียร์ของ snRNA-seq พิสูจน์ได้ว่ามีประโยชน์อย่างยิ่งสำหรับตัวอย่างที่มีปัญหาในการวิเคราะห์โดยใช้วิธี scRNA-seq แบบเดิมๆ. เนื้อเยื่อบางประเภทก่อให้เกิดปัญหาทางเทคนิคเนื่องจากคุณสมบัติ เช่น องค์ประกอบของเมทริกซ์ที่มีความหนาแน่น, ความเปราะบางเมื่อแยกตัวออกจากกัน, หรือไม่เข้ากันกับการบำบัดด้วยเอนไซม์ที่จำเป็นสำหรับการแยกเซลล์เดี่ยว. ตัวอย่างที่เก็บถาวรที่เก็บรักษาไว้ผ่านการตรึงยังทำให้เกิดความท้าทายเช่นกัน.
snRNA-seq ใช้ในการศึกษาเนื้อเยื่อหัวใจของสัตว์เลี้ยงลูกด้วยนมอย่างไร?
เนื้อเยื่อหัวใจของสัตว์เลี้ยงลูกด้วยนมเป็นตัวอย่างของระบบที่ยากต่อ scRNA-seq แต่ยังคล้อยตามการวิเคราะห์ snRNA-seq. เซลล์กล้ามเนื้อหัวใจก่อให้เกิดเครือข่ายที่เชื่อมต่อกันอย่างซับซ้อน ซึ่งไม่สามารถถูกรบกวนได้ง่ายโดยไม่เกิดความเสียหายต่อเซลล์. อย่างไรก็ตาม, ใน 2020 นักวิจัยชาวเยอรมันประสบความสำเร็จในการจัดลำดับหัวใจของสัตว์เลี้ยงลูกด้วยนมที่โตเต็มวัยดวงแรกโดยใช้ snRNA-seq. โดยการแยกนิวเคลียสแทนคาร์ดิโอไมโอไซต์ทั้งหมด, พวกเขาได้รับการกระจายเชิงปฏิบัติของประชากรเซลล์ที่โดดเด่นภายในกล้ามเนื้อหัวใจ. การทำโปรไฟล์ตามขนาดดังกล่าวจะไม่สามารถทำได้ด้วยวิธี scRNA-seq.
snRNA-seq มีประโยชน์ต่อการศึกษาประชากรเซลล์ประสาทอย่างไร?
ประชากรของเซลล์ประสาทเป็นตัวแทนของอีกคลาสหนึ่งที่ได้รับประโยชน์จากความสามารถ snRNA-seq. สมองประกอบด้วยเซลล์ประสาทที่มีสายอย่างประณีตซึ่งไม่แยกออกจากกันเป็นเซลล์เดี่ยวที่สมบูรณ์. การพยายามทำเช่นนั้นอาจทำให้การตอบสนองต่อความเครียดบิดเบือนผลลัพธ์ได้. อย่างไรก็ตามการศึกษาความแตกต่างของการถอดเสียงของชนิดย่อยของระบบประสาทแจ้งความเข้าใจของเราเกี่ยวกับชีววิทยาทางระบบประสาท, กลไกการเกิดโรค, และอื่น ๆ. โปรโตคอล SnRNA-seq ที่ปรับให้เหมาะสมสำหรับเนื้อเยื่อของระบบประสาทส่วนกลางจะรักษาตัวอย่างสมองมนุษย์ที่เก็บถาวรและผ่าตัดใหม่ด้วยความละเอียดเซลล์เดียว.
snRNA-seq ช่วยให้สามารถวิเคราะห์ตัวอย่างทางคลินิกที่ถูกแช่แข็งได้อย่างไร?
ตัวอย่างทางคลินิกที่ถูกแช่แข็งก็มีข้อจำกัดที่เอาชนะโดย snRNA-seq ในทำนองเดียวกัน. การศึกษาโรคตับเปรียบเทียบนิวเคลียสของปอดที่มีสุขภาพดีและนิวเคลียสของไฟโบรติกที่ตรวจพบผ่าน snRNA-seq เผยให้เห็นการระบุประเภทเซลล์ที่เป็นส่วนประกอบอย่างเป็นกลาง. การวิเคราะห์ตัวอย่างทางชีวภาพของผู้ป่วยที่เก็บถาวรดังกล่าวถูกแยกออกจากการวิเคราะห์ก่อนหน้านี้เนื่องจากข้อจำกัดอินพุต scRNA-seq. ขณะนี้นักวิจัยสามารถนำ 'ข้อมูลเชิงลึกแบบโอมิกส์ไปใช้กับตัวอย่างในโลกแห่งความเป็นจริงที่หลากหลายมากขึ้น ซึ่งมีอิทธิพลต่อการวินิจฉัยและการรักษาที่แม่นยำ.
โปรโตคอล snRNA-seq ลดการรบกวนจากการถอดเสียงได้อย่างไร?
ข้อได้เปรียบที่สำคัญของ snRNA-seq อยู่ที่โปรโตคอลการแยกตัวที่อ่อนโยนกว่า ซึ่งขัดขวางปัญหาทางเทคนิคที่เกิดจากความร้อน, ระยะเวลาฟักตัวนานขึ้นหรือการบำบัดด้วยเอนไซม์มากเกินไป. สั้นๆ, วิธีการสลายแบบอ่อนที่ใช้สำหรับการแยกนิวเคลียร์จะป้องกันการเปลี่ยนแปลงการถอดรหัสที่เกิดจากความเครียดซึ่งอาจบิดเบือนผลลัพธ์ของ scRNA-seq. โดยไม่ต้องให้เซลล์ที่ไม่บุบสลายเข้าสู่ขั้นตอนการแยกตัวที่รุนแรง, การสุ่มตัวอย่าง snRNA-seq จะรักษาความสมบูรณ์ของการถอดเสียงที่มีอยู่ในขณะที่แยกตัวได้ดีขึ้น.
snRNA-seq ลดรูปแบบการแสดงออกของยีนปลอมได้อย่างไร?
วิธีนี้จะช่วยลดการเกิดรูปแบบการแสดงออกของยีนปลอมที่เกิดจากกระบวนการแยกตัวออกไปให้เหลือน้อยที่สุด. ไรโบโซมที่เจริญเต็มที่พบได้ภายในช่องไซโตพลาสซึมเท่านั้น หมายความว่า mRNA ใดๆ ที่เข้ารหัสยีนตอบสนองต่อความเครียดทันทีถึงเร็วที่แสดงออกมาหลังการแยกตัวไม่สามารถแปลได้. เป้าหมายการถอดเสียงแบบดาวน์สตรีมของพวกเขาจึงยังคงไม่มีการเปลี่ยนแปลง. การศึกษาเปรียบเทียบที่ใช้ทั้งสองเทคนิคกับเนื้อเยื่อเดียวกันแสดงให้เห็นว่า snRNA-seq จับชุดย่อยของเซลล์ประเภทที่กว้างขึ้นโดยมีการรบกวนจากการถอดรหัสที่เกิดจากการแยกตัวน้อยกว่า.
ระยะเวลาการสลายสั้น ๆ ช่วยควบคุมอคติของการถอดรหัสใน snRNA-seq ได้อย่างไร?
ปัจจัยเพิ่มเติม เช่น ระยะเวลาการสลายที่สั้น ช่วยควบคุมอคติของการถอดเสียง. การสัมผัสกับน้ำแข็งเป็นเวลานานก่อนที่จะดำเนินการเตรียมห้องสมุดนิวเคลียสเดี่ยวอาจส่งผลเสียต่อคุณภาพข้อมูลโดยการเริ่มต้นการเปลี่ยนแปลงการถอดเสียง. การกำหนดเวลาอย่างระมัดระวังจะช่วยลดผลกระทบดังกล่าว. ปริมาณเนื้อเยื่อเริ่มต้นที่เพียงพอยังรับประกันการเตรียมนิวเคลียสคุณภาพสูงที่จำเป็นสำหรับการทำโปรไฟล์ที่แข็งแกร่งเนื่องจากข้อจำกัดด้านระเบียบวิธี.
เวิร์กโฟลว์ snRNA-seq ที่ได้รับการปรับปรุงให้เหมาะสมจะลดข้อผิดพลาดทางเทคนิคได้อย่างไร?
โดยรวม, เวิร์กโฟลว์ snRNA-seq ที่ได้รับการปรับปรุงให้เหมาะสมจะช่วยลดปัจจัยก่อนการวิเคราะห์ที่ทำให้การตีความทางชีววิทยาซับซ้อนลง. การสกัดเนื้อหานิวเคลียร์อย่างอ่อนโยนทำให้เกิดโปรไฟล์การแสดงออกของยีนที่มีรูปร่างน้อยกว่าโดยสิ่งประดิษฐ์ทางเทคนิคมากกว่ากระบวนการทางชีววิทยาภายนอก. สิ่งนี้ทำให้เกิดความชัดเจนและความมั่นใจมากขึ้นในการค้นพบที่รวบรวมเกี่ยวกับเครือข่ายการกำกับดูแล, ประชากรย่อยที่หายาก, และโปรแกรมความเชี่ยวชาญด้านเซลล์ภายในระบบที่ซับซ้อนในวิฟ.
นักวิจัยสามารถใช้ snRNA-seq เพื่อพัฒนาความเข้าใจทางชีววิทยาได้อย่างไร?
เป็นเทคนิคที่เป็นนวัตกรรมใหม่ที่ขัดเกลามุมมองของเราเกี่ยวกับความซับซ้อนของเซลล์, snRNA-seq เปิดขอบเขตใหม่สำหรับการใช้งานด้านการวิจัยที่หลากหลาย. ตัวอย่างบางส่วนเน้นย้ำถึงศักยภาพในการขับเคลื่อนความก้าวหน้าทางวิทยาศาสตร์:
- ชีววิทยาพัฒนาการ: การเปรียบเทียบนิวเคลียสจากระยะตัวอ่อนที่แตกต่างกันสามารถเปิดเผยโปรแกรมการกำกับดูแลเฉพาะระยะที่ชี้แนะความแตกต่าง. การไล่ระดับสีพัฒนาการของการทำแผนที่ snRNA-seq ที่ได้รับการแก้ไขเชิงพื้นที่อาจเปิดเผยกลไกการกำหนดรูปแบบ.
- พยาธิวิทยาของโรค: การทำโปรไฟล์ที่เป็นโรคกับนิวเคลียสของเนื้อเยื่อที่มีสุขภาพดีอาจระบุการเปลี่ยนแปลงที่เกี่ยวข้องกับพยาธิวิทยาในเซลล์ชนิดหายากที่ส่องสว่างกลไกของโรค. การวิเคราะห์ตัวอย่างผู้ป่วยสามารถให้ข้อมูลการวินิจฉัยและการรักษาที่แม่นยำ.
- ประสาทจิตเวช: การตรวจสอบเนื้อเยื่อสมองหลังการชันสูตรที่เก็บถาวรผ่านทาง snRNA-seq ช่วยระบุลักษณะความหลากหลายทางระบบประสาทของภาวะทางจิตเวช. การศึกษาระยะยาวอาจเปิดเผยตัวบ่งชี้ทางชีวภาพตามยาวและเป้าหมายในการรักษา.
- การศึกษาเชิงวิวัฒนาการ: SnRNA-seq ทำให้การเปรียบเทียบข้ามสายพันธุ์ที่เป็นไปได้ซึ่งก่อนหน้านี้มีความท้าทายเนื่องจากความแตกต่างระหว่างสิ่งมีชีวิตในคุณสมบัติของเนื้อเยื่อ. เช่น “ไฟโล-snRNA-seq” แจ้งความเข้าใจของเราเกี่ยวกับกระบวนการกำกับดูแลแบบอนุรักษ์และแบบแตกต่าง.
- การบูรณาการหลายโอมิกส์: การจับคู่ snRNA-seq กับเทคนิคการทำโปรไฟล์เชิงพื้นที่ทำให้ได้แผนที่ epigenomic และ transcriptomic ที่ได้รับการแก้ไขเชิงพื้นที่เพื่ออธิบายสภาพแวดล้อมไมโครนิวเคลียร์. การบูรณาการข้อมูลการถอดเสียงเชิงพื้นที่เข้ากับชั้นโปรตีโอมิกหรือเมแทบอลิซึมจะให้บริบทระดับระบบ.
สรุป
เนื่องจากเป็นหนึ่งในเทคนิคใหม่ๆ มากมายที่ปฏิวัติการวิเคราะห์เซลล์เดียว, snRNA-seq กระตุ้นการค้นพบโดยทำให้ตัวอย่างที่ยากก่อนหน้านี้สามารถทดลองได้. การขยายขนาดของ omics นิวเคลียร์รับประกันข้อมูลเชิงลึกที่สดใหม่ในการพัฒนาสาขาที่หลากหลายตั้งแต่เวชศาสตร์ฟื้นฟูไปจนถึงเนื้องอกวิทยาที่มีความแม่นยำ. พร้อมด้วยแนวทางเสริม, snRNA-seq ช่วยคลี่คลายความซับซ้อนอันน่าทึ่งของชีวิตในระดับที่ไม่เคยมีมาก่อน.